Como es sabido, en los seres humanos el sexo femenino es determinado cromosómicamente, siendo el homogamético. Por ello, las hembras serán XX.
En ocasiones, ocurren cambios cromosómicos numéricos, más concretamente, aneuploidía. Estas aneuploidias son más comunes en plantas; sin embargo, en humanos se han detectado monosomías y trisomías. Estas trisomías pueden ser en cromosomas autosómicos, dando lugar a enfermedades como el síndrome de Down o en cromosomas sexuales, dando lugar a mujeres con XXX, vulgarmente conocidas como “las superhembras”.
El síndrome triple X es una anomalía cromosómica relativamente frecuente. Sin embargo, no suele identificarse en el nacimiento al no presentar un fenotipo característico. Normalmente, el diagnóstico se realiza cuando la mujer presenta una insuficiencia ovárica primaria. Sin embargo, en ocasiones, provoca retraso mental tanto profundo como ligero, malformaciones en la cara y aparato genitourinario o cardiopatías.
En todas las mujeres, siempre se inactiva por azar uno de los dos cromosomas X. Esto ocurre aleatoriamente de forma temprana durante la biogénesis y es controlada por el centro de inactivación cromosoma X. Por ello, sólo un cromosoma X de cada célula está activo genéticamente y el otro está inactivo. Sin embargo, aproximadamente un 5-10% de genes del cromosoma X que se debieron inactivar, no lo hacen. Además, las regiones psudoautosómicas del cromosoma X no se inactivan.
En caso de contar con la trisomía X, se inactivan dos de los tres cromosomas. Pero las partes no inactivadas del cromosoma X son expresados por los tres cromosomas X y, por ello, hay una sobrexpresión de genes.
Aún hay muchas cuestiones no resueltas en la trisomía X, por ello, es necesario seguir investigando sobre la fisiopatología y el mecanismo genético involucrado en los problemas médicos asociados.
Referencias:
https://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1699-695X2011000200012
https://www.orpha.net/data/patho/Pro/es/TrisomiaX_OJRD_Spanish.pdf
Mes: enero 2022
Vacuna experimental, basada en la misma tecnología de las vacunas de Moderna o Pfizer frente a SARS-CoV-2, muestra resultados prometedores en ratones y primates no humanos para la infección por VIH
El pasado mes de junio se cumplieron 40 años de los primeros casos de infección oficial causada por el VIH. A lo largo de todo este tiempo esta infección que genera un síndrome de inmunodeficiencia adquirida se ha cobrado la vida de mas de 30 millones de personas.
En la actualidad se ha avanzado bastante en los tratamientos antivirales frente al VIH hasta conseguir incluso su control en gran parte de los pacientes. Sin embargo no se ha logrado desarrollar una vacuna que proteja contra la enfermedad como si se ha obtenido para muchas otras enfermedades infecciosas.
A día de hoy se están realizando ensayos en diferentes animales con un prototipo de vacuna cuya tecnología se basa en lo mismo que dos de las vacunas para COVID-19.
Primeramente ¿Qué es el VIH?
El VIH pertenece a la familia de los lentivirus y se clasifica en dos tipos: VIH-1 y VIH-2 que tienen un 40-50% de homología genética y cuentan con una organización genómica similar. Tanto el VIH-1 como el VIH-2 provienen de diferentes saltos inter-especie de virus que infectan en la naturaleza
Al igual que en todos los virus envueltos, la envoltura consiste en una bicapa lipídica,en esta envoltura se encuentran presentes algunas proteínas de la célula huésped y muy significativamente Env, la glicoproteína de envoltura del VIH. Env se encuentra anclada en la membrana y consiste en un hetero-trímero formado por tres moléculas llamadas glicoproteína 120 (gp120).
La dificultad de neutralizar la infección por VIH-1 reside en la proteína Env; ya que cuenta con gran variabilidad de la envoltura con 5 regiones hipervariables además de un alto nivel de glicosilación de Env impidiendo la unión de anticuerpos y por ultimo enmascaramiento conformacional, término que describe que el sitio de unión con los co-receptores (CCR5 ó CXCR4), no existe hasta que se organiza espacialmente después del cambio en la conformación y es por tanto muy poco susceptible a la neutralización mediada por anticuerpos
Y por otro lado el gen gag codifica las principales proteínas estructurales
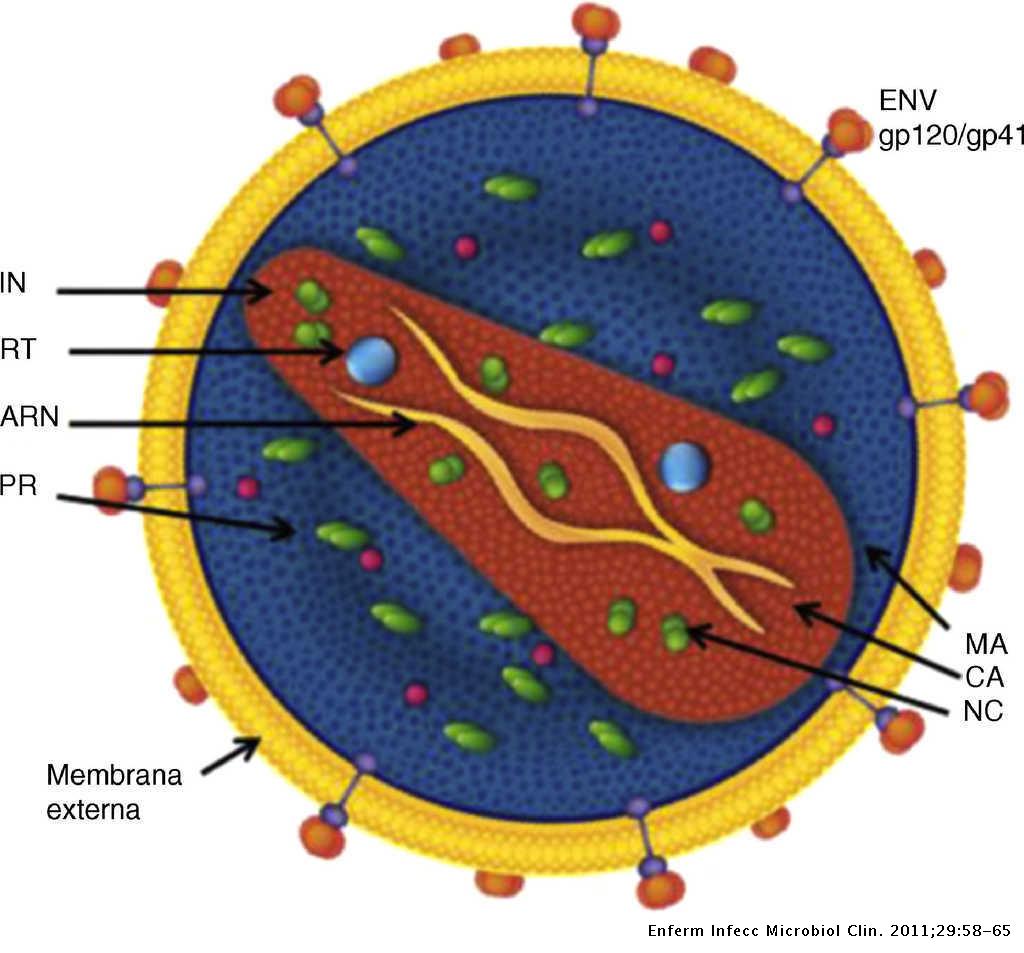
Al igual que con las vacunas contra el covid-19, la vacuna experimental contra el VIH envía instrucciones a las células, para producir dos proteínas clave del virus del VIH (Env y Gag).
“Esta vacuna experimental de ARN mensajero combinas múltiples características que podrían superar las limitaciones de otras vacunas experimentales para el VIH por lo que representa una aproximación prometedora”, ha señalado Anthony Fauci, Director del del Instituto Nacional de Alergias y Enfermedades Infecciosas, institución que junto a la empresa Moderna Inc (empresa responsable de una de las vacunas de ARN para COVID-19) y otros centros ha liderado la investigación.
El funcionamiento de la vacuna se rige por nanopartículas lipídicas que contienen en su interior moléculas de ARN mensajero de dos proteínas virales.
Una vez en el interior de las células este ARN mensajero inoculado por medio de la vacuna se traduce en las dos proteínas del virus formando así partículas virales no infecciosas que permiten una respuesta optima del sistema inmunitario.
Los resultados en ratones tras dos inyecciones de la vacuna mostraron anticuerpos neutralizantes en todos ellos (prueba de la respuesta inmunitaria) y por tanto se decidió pasar a una similar del ser humano, los primates. Primeramente recibieron una única dosis y se fueron administrando dosis posteriores a lo largo del año, sin mayores complicaciones salvo la pérdida de apetito de los macacos.
Tras 14 meses desde la primera dosis todos los individuos vacunados habían alcanzado unos niveles de anticuerpos neutralizantes bastante altos y dirigidos hacia la gran mayoría de cepas del VIH. Además de los niveles de anticuerpo, fortaleció la actividad de las células T de los monos contra este virus infeccioso que son claves en la respuesta inmunitaria. Al ser expuestos semanalmente a SHIV, 2 de cada siete no estaban infectados por lo que los investigadores concluyeron:
»No es un resultado rotundo, pero muestra que el enfoque podría funcionar en principio»
Por lo que este proyecto ofrece un punto de partida prometedor para un desarrollo exitoso de vacunas contra el VIH
“Estamos refinando nuestro protocolo de la vacuna para mejorar la calidad y la cantidad de partículas víricas producidas”, ha señalado Paolo Lusso. “Esto podría aumentar más la eficacia de la vacuna y reducir el número de inoculaciones primarias y de recuerdo necesarias para producir una respuesta inmunitaria robusta”, indica el investigador.
Una vez confirmada la seguridad y eficacia de la vacuna, el siguiente paso que quieren llevar a cabo es un ensayo en fase 1 con voluntarios humanos.
https://genotipia.com/genetica_medica_news/vacuna-vih-arn-mensajero/
HEMOFILIA A
La hemofilia es una enfermedad de origen genético conocida desde hace siglos. Está ligada al sexo, concretamente al cromosoma X, la cual genera trastornos en la coagulación sanguínea. Esto hace que aumente la tendencia del paciente a sufrir hemorragias. Existen tres tipos de hemofilia: A, B y C. Nos centraremos en la hemofilia A ya que es la más frecuente entre la población, con una incidencia de 1/5000 niños varones. Este tipo de hemofilia representa el 80 % de los casos diagnosticados, siendo la patología ligada al cromosoma X más frecuente.
La causa de esta enfermedad se debe a una mutación en el gen F8 (localizado en el cromosoma X), el cual se codifica para la proteína del factor de coagulación VIII. Con esta mutación puede alterarse el factor o reducirse a una cantidad inferior a la requerida por el organismo. Por lo general los pacientes que sufren esta enfermedad tienen antecedentes familiares aunque también pueden darse mutaciones de novo.
La hemofilia A presenta un patrón hereditario recesivo ligado al sexo, donde los factores de coagulación VIII y IX se encuantran alterados ocasionando déficit cuantitativo y funcional en la formación de coágulos sanguíneos. Tan solo se presenta en los hombres, mientras que las mujeres generalmente son portadoras aunque pueden manfiestar la enfermedad en casos de inactivación del cromosoma X. Debido al estado homocigoto del cromosoma X de los hombres, estos sufren la enfermedad; sin embargo, en las mujeres su condición heterocigota, hace que sean portadoras asintomáticas.
La inactivación del cromosoma X en mujeres sintomáticas y mujeres hemofílicas puede verse afectado por algunos mecanismos genéticos que desencadenan efectos relevantes en las mujeres portadoras. Algunas mujeres portadoras pueden ser sintomáticas y presentar episodios hemorrágicos en algunas ocasiones, como hematomas. Estos se encuentran directamente relacionados con los niveles en el plasma sanguíneo de factor VIII (hemofilia A) o IX (hemofilia B).
Para detectar la enfermedad se empelan diversas técnicas de laboratorio que miden los niveles normales y alterados de actividad plasmática de los factores de coagulación VIII y IX. El síntoma más comun es la hemorragia, cuya gravedad depende del nivel del factor VIII presente en el plasma. Generalmente estos episodios se dan a consecuencia de traumas en articulaciones (hemartrosis) , músculos y zonas vinculadas al SNC, generando lesiones en vasos sanguíneos. Otro tipo de hemorragias comunes incluyen: SNC, sistema gastrointestinal, sistema genital-urinario, mucosas nasal y hematomas en vías respiratorias.
Hemorragias típicas en hemofilia
Los principales tratamientos se enfocan en prevenir la hemorragia y revertir sus efectos, ya que esta enfermedad por el momento no tiene cura definitiva. Algunos son tratamientos profilácticos primarios a edades tempranas. Otros consisten en reposición a niveles adecuados del factor de coagulación deficitario en función del tipo de hemofilia, generalmente de manera intravenosa. También es necesario el uso de medicamentos como DDAVP (acetato de desmopresina) que estimula la liberación del F8 y ácido épsilon aminocaproico que previne que los coágulos se deshagan.
Referencias:
https://www.cdc.gov/ncbddd/spanish/hemophilia/treatment.html
https://cefegen.es/blog/hemofilia-a-genetica-causas-sintomas-y-tratamiento
Artículo: Hemofilia: abordaje diagnóstico y terapéutico. Lina María Martínez-Sánchez, Luis Felipe Álvarez-Hernández
Mª Victoria Montoza del Pino, 2º Biología.